Cantitatea de căldură care trebuie raportată la Universitate în echilibru izobar-izoterm. proces pentru a-l transfera de la tv. (crist.) în lichid (aceeași cantitate de căldură este eliberată în timpul cristalizării v-va). T. p. Este un caz special al căldurii unei tranziții de fază.
Distingeți bătăile. T. p. (Măsurat în J / kg, kcal / kg) și molar (molar) T. p. (J / mol). În tabel. se dau valori ale bătăilor. T. p. Lpl la atm. presiune de 760 mm RT. Art. (sau 101 325 Pa) și punctul de topire Tm.
Dicționar enciclopedic fizic. - M .: Enciclopedia sovietică. . 1983 .
Cantitatea de căldură care trebuie raportată la substanța aflată în echilibru izobar-izoterm. proces pentru a-l transfera complet din cristalin solid. stare la lichid. T. p. Este egală cu cantitatea de căldură degajată în timpul cristalizării unei substanțe din faza lichidă. T. L PL pentru anumite substanțe la presiune normală (1013,25 hPa) și punct de topire T pl.
Enciclopedia fizică. În 5 volume. - M .: Enciclopedia sovietică. Redactor șef A. M. Prokhorov. 1988 .
Vedeți ce este „HEAT OF MELTING” în alte dicționare:
Cantitatea de căldură care trebuie comunicată unei substanțe cristaline solide la presiune constantă pentru a o transfera complet într-o stare lichidă. Căldura de fuziune per unitate de masă a unei substanțe se numește căldură specifică de fuziune. * * * ... ... Dicționar enciclopedic
Cantitatea de căldură care trebuie comunicată unei substanțe cristaline solide la o presiune constantă pentru a o transfera complet într-o stare lichidă. Căldura de fuziune a unei unități de masă a unei substanțe se numește căldură specifică de fuziune ... Mare dicționar enciclopedic
căldură de fuziune - cantitatea de căldură necesară unei substanțe aflate într-un proces izoberic de echilibru izoterm pentru a trece de la o stare solidă (cristalină) la o stare lichidă (aceeași cantitate de căldură este eliberată în timpul cristalizării unei substanțe). Căldura ... ... Dicționar enciclopedic al metalurgiei
Cantitatea de căldură care trebuie comunicată unei substanțe într-un proces de echilibru pentru a o transfera dintr-o stare solidă (cristalină) într-o stare lichidă (aceeași cantitate de căldură este eliberată în timpul cristalizării unei substanțe). Căldura fuziunii ... ... Dicționar metalurgic
căldură de fuziune - lydymosi šiluma statusas T sritis Standartizacija ir metrologija apibrėžtis Šilumos kiekis, reikalingas medžiagai išlydyti. atitikmenys: angl. căldură de fuziune; topirea căldurii vok. Schmelzwärme, fr. căldură de fuziune, f pranc. chaleur de fusion, f ... Penkiakalbis aiškinamasis metrologijos terminų žodynas
căldură de fuziune - lydymosi šiluma statusas T sritis chemija apibrėžtis Šilumos kiekis, reikalingas medžiagai išlydyti. atitikmenys: angl. căldură de fuziune; topind căldura rusă. căldură de fuziune ... Chemijos terminų aiškinamasis žodynas
căldură de fuziune - lydymosi šiluma statusas T sritis fizika atitikmenys: angl. căldură de fuziune; topirea căldurii vok. Schmelzwärme, fr. căldură de fuziune, f pranc. chaleur de fusion, f ... Fizikos terminų žodynas
căldură de fuziune - lydymosi šiluma statusas T sritis Energetika apibrėžtis Šiluma, reikalinga kietai kristalinei medžiagai paversti skysčiu, esant pastoviai lydymosi temperatureūrai. Būna savitoji ir molinė lydymosi šiluma. Jų matavimo vienetai - džaulis kilogramui ... ... Aiškinamasis šiluminės ir branduolinės technikos terminų žodynas
Cantitatea de căldură care trebuie comunicată unei substanțe într-un procedeu de echilibru izoterm izobar, pentru a o transfera dintr-o stare solidă (cristalină) într-un lichid (aceeași cantitate de căldură este eliberată în timpul cristalizării ... Marea enciclopedie sovietică
Miza cu căldură, este necesar să spui un televizor unui roi cristalin. în wu la post. presiune pentru a-l transfera complet într-o stare lichidă. T. p. Unități de masă în wa. specifice T. p ... Istoria naturală. Dicționar enciclopedic
cărți
- Proprietățile mecanice ale metalelor lichide. Proprietăți extreme ale cristalelor minime de metale, O.S. Nikolaev. Această carte este în două părți. Prima parte descrie metoda termică pentru evaluarea proprietăților mecanice ale metalelor lichide. Se aplică organismelor din oricare dintre cele trei state. Primit ...
Toată lumea știe că apa poate fi în natură în trei stări de agregare - solid, lichid și gazos. În timpul topirii, gheața solidă se transformă în lichid, iar la încălzirea ulterioară, lichidul se evaporă, formând vapori de apă. Care sunt condițiile de topire, cristalizare, evaporare și condensare a apei? La ce temperatură se formează gheața sau se formează aburi? Vom vorbi despre acest lucru în acest articol.
Asta nu înseamnă că vaporii de apă și gheața sunt rare în viața de zi cu zi. Cu toate acestea, cea mai frecventă este tocmai starea lichidă - apa obișnuită. Experții au descoperit că pe planeta noastră există peste 1 miliard de kilometri cubi de apă. Cu toate acestea, nu mai mult de 3 milioane km 3 de apă aparțin corpurilor de apă dulce. O cantitate suficient de mare de apă dulce „se odihnește” în ghețari (aproximativ 30 de milioane de kilometri cubi). Cu toate acestea, a topi gheața unor astfel de blocuri imense este departe de a fi ușor. Restul apei este sărat, aparținând mărilor oceanelor.
Apa înconjoară omul modern peste tot, în timpul majorității procedurilor zilnice. Mulți oameni cred că rezervele de apă sunt inepuizabile, iar umanitatea poate folosi întotdeauna resursele hidrosferei terestre. Totuși, acest lucru este departe de caz. Resursele de apă ale planetei noastre sunt epuizate treptat și este posibil ca după câteva sute de ani de apă dulce pe Pământ să nu rămână deloc. Prin urmare, absolut orice persoană trebuie să fie atentă la apa dulce și să o economisească. Până la urmă, chiar și în vremea noastră există state în care aprovizionarea cu apă este catastrofal mică.
Proprietățile apei

Înainte de a vorbi despre temperatura de topire a gheții, merită să aveți în vedere proprietățile de bază ale acestui lichid unic.
Deci, următoarele proprietăți sunt inerente în apă:
- Lipsa de culoare.
- Lipsa de miros.
- Lipsa gustului (cu toate acestea, apa potabilă de calitate are un gust bun).
- Transparență.
- Fluiditatea.
- Capacitatea de a dizolva diverse substanțe (de exemplu, săruri, alcaline etc.).
- Apa nu are propria formă permanentă și este capabilă să ia forma unui vas în care cade.
- Capacitatea de a fi curățat prin filtrare.
- Când este încălzită, apa se extinde și, atunci când este răcită, se contractă.
- Apa se poate evapora, transformându-se în aburi și înghețând pentru a forma gheață cristalină.
Această listă prezintă proprietățile de bază ale apei. Acum vom înțelege care sunt caracteristicile stării solide de agregare a acestei substanțe și la ce temperatură se topește gheața.

Gheața este o substanță solidă cristalină care are o structură destul de instabilă. La fel ca apa, este transparentă, nu are culoare și miros. Gheața are, de asemenea, proprietăți precum fragilitatea și alunecarea; Este rece la atingere.
Zăpada reprezintă și apa înghețată, dar are o structură liberă și are culoare albă. Zăpada care cade în fiecare an în majoritatea țărilor lumii.
Atât zăpada, cât și gheața sunt substanțe extrem de volatile. Pentru a topi gheața, nu trebuie să depuneți mult efort. Când începe să se topească?

În natură, gheața tare există doar la temperaturi de 0 ° C și mai mici. Dacă temperatura ambiantă crește și devine mai mare de 0 ° C, gheața începe să se topească.
La temperatura de topire a gheții, la 0 ° C, are loc un alt proces - înghețarea sau cristalizarea apei lichide.
Acest proces poate fi observat de toți locuitorii climatului temperat temperat. În timpul iernii, când temperatura exterioară scade sub 0 ° C, adesea cad suficientă zăpadă care nu se topește. Iar apa lichidă care se afla pe străzi îngheață, transformându-se în zăpadă solidă sau gheață. Primăvara, puteți vedea procesul invers. Temperatura ambientală crește, astfel încât gheața și zăpada se topesc, formând numeroase bălți și noroi, ceea ce poate fi considerat singurul minus al încălzirii primăverii.
Astfel, putem concluziona că, la ce temperatură începe să se topească gheața, la aceeași temperatură, începe procesul de înghețare a apei.
Cantitatea de căldură

Într-o știință precum fizica, deseori este utilizat conceptul de cantitate de căldură. Această valoare arată cantitatea de energie necesară pentru încălzire, topire, cristalizare, fierbere, evaporare sau condensarea diferitelor substanțe. Mai mult, fiecare dintre aceste procese are propriile sale caracteristici. Să vorbim despre câtă căldură este necesară pentru încălzirea gheții în condiții normale.
Pentru a încălzi gheața, mai întâi trebuie să o topiți. Aceasta necesită cantitatea de căldură necesară pentru a topi solidul. Căldura este egală cu produsul din masa de gheață și căldura specifică a topirii sale (330-345 mii Joule / kg) și este exprimată în Joules. Să presupunem că ni se administrează 2 kg de gheață tare. Astfel, pentru a-l topi, avem nevoie de: 2 kg * 340 kJ / kg \u003d 680 kJ.
După aceea, trebuie să încălzim apa formată. Cantitatea de căldură pentru acest proces va fi puțin mai dificil de calculat. Pentru a face acest lucru, trebuie să cunoașteți temperatura inițială și finală a apei încălzite.
Deci, să spunem că trebuie să încălzim apa rezultată din topirea gheții la 50 ° C. Adică, diferența dintre temperatura inițială și cea finală \u003d 50 ° C (temperatura inițială a apei - 0 ° C). Apoi, ar trebui să înmulțiți diferența de temperatură cu masa de apă și căldura specifică, care este de 4.200 J * kg / ° C. Adică cantitatea de căldură necesară pentru încălzirea apei \u003d 2 kg * 50 ° C * 4.200 J * kg / ° C \u003d 420 kJ.
Apoi obținem asta pentru a topi gheața și apoi a încălzi apa rezultată, avem nevoie de: 680.000 J + 420.000 J \u003d 1.100.000 Joule, sau 1.1 Megajoules.
Cunoscând temperatura la care se topește gheața, se pot rezolva multe probleme dificile în fizică sau chimie.
În concluzie
Deci, în acest articol am aflat câteva fapte despre apă și cele două stări agregate ale acesteia - solid și lichid. Cu toate acestea, vaporii de apă sunt un subiect la fel de interesant de studiat. De exemplu, în atmosfera noastră conțin aproximativ 25 * 10 16 metri cubi de vapori de apă. În plus, spre deosebire de îngheț, evaporarea apei are loc la orice temperatură și se accelerează atunci când este încălzită sau în prezența vântului.
Am aflat la ce temperatură se topește gheața și îngheață apa lichidă. Asemenea fapte ne vor fi întotdeauna utile în viața de zi cu zi, deoarece apa ne înconjoară peste tot. Este important să ne amintim mereu că apa, în special apa dulce, este resursa epuizabilă a Pământului și trebuie tratată cu grijă.
În fizică, topirea este tranziția unei substanțe de la un solid la o stare lichidă. Exemple clasice ale procesului de topire sunt topirea gheții și transformarea unei bucăți solide de staniu în lipit lichid atunci când este încălzită cu un fier de lipit. Transferul unei anumite cantități de căldură către corp duce la o schimbare a stării sale de agregare.
De ce solidul devine lichid?
Încălzirea unui solid duce la o creștere a energiei cinetice a atomilor și moleculelor, care la temperatura normală sunt situate în mod clar în nodurile zăbrelei de cristal, ceea ce permite corpului să mențină o formă și o dimensiune constantă. Când sunt atinse unele valori critice ale vitezei, atomii și moleculele încep să își părăsească locurile, legăturile se rup, corpul începe să-și piardă forma - devine lichid. Procesul de topire nu are loc brusc, ci treptat, astfel încât de ceva timp componentele solide și lichide (fazele) sunt în echilibru. Topirea se referă la procesele endotermice, adică la cele care apar cu absorbția căldurii. Procesul opus atunci când lichidul se solidifică se numește cristalizare.

Fig. 1. Tranziția unei stări solide, cristaline a unei substanțe într-o fază lichidă.
S-a constatat că până la sfârșitul procesului de topire, temperatura nu se schimbă, deși căldura este furnizată tot timpul. Nu există nicio contradicție aici, deoarece energia primită în această perioadă de timp este cheltuită pentru ruperea legăturilor de cristal ale zăbrelei. După distrugerea tuturor legăturilor, fluxul de căldură va crește energia cinetică a moleculelor și, prin urmare, temperatura va începe să crească.

Fig. 2. Graficul temperaturii corpului comparativ cu timpul de încălzire.
Determinarea căldurii specifice de fuziune
Căldura specifică de fuziune (denumire - litera greacă „lambda” - λ) este o cantitate fizică egală cu cantitatea de căldură (în jouli) care trebuie transferată la o masă solidă de 1 kg pentru a o transfera complet în faza lichidă. Formula specifică de căldură a fuziunii este următoarea:
$$ λ \u003d (Q \\ peste m) $$
m este masa substanței care se topește;
Q este cantitatea de căldură transferată substanței în timpul topirii.
Valorile diferitelor substanțe sunt determinate experimental.
Cunoscând λ, putem calcula cantitatea de căldură care trebuie raportată unui corp de masă m pentru topirea sa completă:
În ce unități se măsoară căldura specifică de fuziune
Căldura specifică de fuziune în SI (Sistemul Internațional) se măsoară în jouli pe kilogram, J / kg. Pentru unele sarcini, se folosește o unitate de măsură din afara sistemului - kilocalorii pe kilogram, kcal / kg. Reamintim că 1 kcal \u003d 4.1868 J.
Căldură specifică de fuziune a anumitor substanțe
Informații despre valorile de căldură specifice pentru o anumită substanță pot fi găsite în directoarele de carte sau în versiunile electronice ale resurselor de internet. De obicei, acestea sunt date sub forma unui tabel:
Căldură specifică de fuziune a substanțelor
Una dintre cele mai refractare substanțe este carbura de tantal - TaC. Se topește la o temperatură de 3990 ° C. Acoperirile TaC sunt utilizate pentru a proteja metalul în matrițele în care sunt turnate piese din aluminiu.

Fig. 3. Procesul de topire a metalului.
Ce am învățat?
Am aflat că trecerea de la solid la lichid se numește topire. Topirea se produce prin transferul de căldură într-un solid. Căldura specifică de fuziune arată câtă căldură (energie) este necesară pentru o substanță solidă care cântărește 1 kg pentru a o transforma într-o stare lichidă.
Test asociat
Raport Evaluare
Evaluare medie: 4.7. Total evaluări primite: 217.

 Pro și contra contra educației sovietice
Pro și contra contra educației sovietice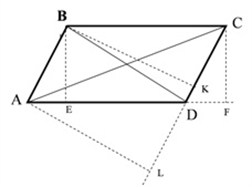 Paralelogramă și proprietățile sale
Paralelogramă și proprietățile sale Probleme de mediu la nivel global
Probleme de mediu la nivel global